Penelitian Vaksin Nusantara Kembali Masuk Jurnal Internasional
Nicolas
Diperbarui
28 Oktober 2022 15:29 WIB
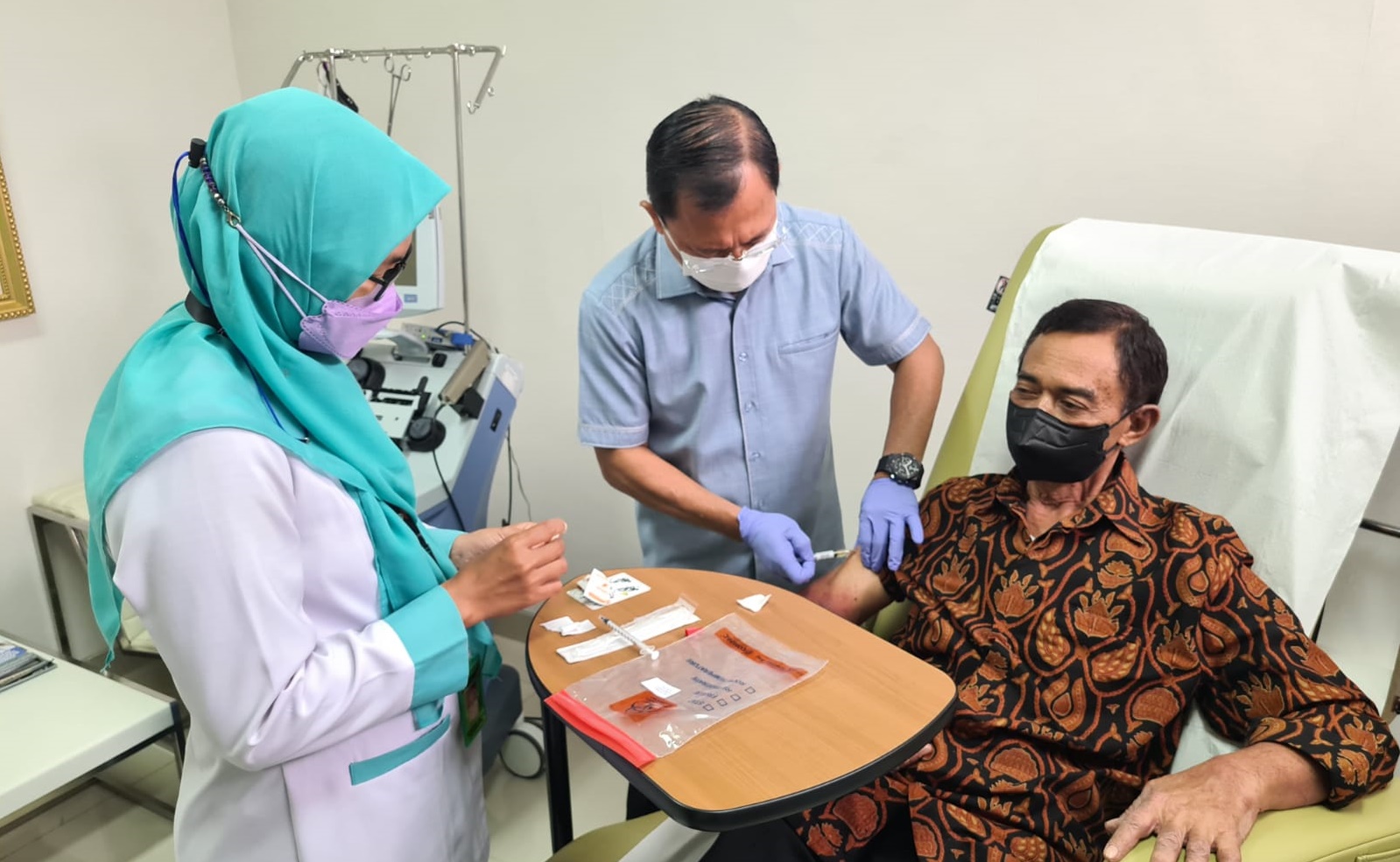
Jakarta, MI- Penelitian Vaksin Nusantara yang digagas mantan Menteri Kesehatan, Terawan Agus Putranto kembali terbit di jurnal ilmiah internasional. Teranyar, penelitian vaksin berbasis sel dentritik itu dipublikasikan di website National Library of Medicine dengan judul "A personal Covid-19 dendritic cell vaccine made at point-of-care: Feasibility, safety, and antigen-specific cellular immune responses"
Ketua Umum Dewan Pimpinan Nasional (DPN) Vox Point Indonesia, Handoyo Budi Sedjati, Jumat (28/10) mengatakan, dengan masuknya kembali Vaksin Nusantara di jurnal medis internasional membuktikan bahwa vaksin hasil karya anak bangsa diakui dunia. Oleh karena itu, Handoyo berharap agar pemerintah Indonesia dapat segera mengeluarkan regulasi agar vaksin covid-19 pertama di dunia yang menggunakan sel dendritik dapat diakses oleh masarakat Indonesia.
"Apalagi tingkat keberhasilan Vaksin Nusantara telah terbukti dapat melindungi diri dari paparan virus corona yang telah bermutasi dalam berbagai varian," kata Handoyo.
Dikatakan, sejumlah anggota masyarakat yang terkena inflamasi paska Covid-19 terbukti dapat disembuhkan usai mendapatkan Vaksin Nusantara.
Sebagaimana dikutip dari website National Library of Medicin, https://pubmed.ncbi.nlm.nih.gov/36018753/, tingkat efikasi dan efektivitas vaksin berbasis sel dendritik mencapai sebesar 96,8% persen.
Penelitian ini bertujuan untuk menetapkan kelayakan vaksin sel dendritik pribadi terhadap protein lonjakan SARS-CoV-2, menetapkan keamanan injeksi vaksin subkutan tunggal, dan menentukan respons imun spesifik antigen setelah vaksinasi.
Pada penelitian fase I sebanyak 31 subjek ditugaskan ke salah satu dari sembilan formulasi sel dendritik dan limfosit (DCL) autologus yang diinkubasi dengan 0,10, 0,33, atau 1,0 g protein lonjakan SARS-CoV-2 rekombinan.
Lalu, dicampur dengan saline atau 250 atau 500 g faktor perangsang koloni granulosit-makrofag (GM-CSF) sebelum injeksi.
Pada Fase 2, 145 subjek diacak ke salah satu dari tiga formulasi yang ditentukan oleh inkubasi dengan tiga jumlah protein lonjakan yang sama tanpa GM-CSF, kemudian dinilai untuk keamanan dan respons seluler. Vaksin berhasil diproduksi untuk setiap subjek di titik perawatan.
Lebih lanjut dalam jurnal itu disebutkan, sekitar 46,4% subjek memiliki efek samping (AE) grade 1; 6,5% memiliki grade 2 AE. Di antara 169 subjek yang dapat dievaluasi, tidak ada alergi akut, grade 3 atau 4, atau AE serius.
Pada fase 1, antibodi domain pengikat anti-reseptor meningkat pada 70% subjek pada hari ke-28.[Lin]
Berita Sebelumnya
Berita Selanjutnya
Berita Terkait

