Jakarta, MI - Badan Pemeriksan Keuangan (BPK) mengungkap indikasi dugaan tindak pidana korupsi di anak perusahaan PT Bio Farma yakni PT Kimia Farma dalam praktik penilaian dan pencatatan obat menjadi impor yang merugikan negara miliaran rupiah.
"Kimia Farma mengalami kerugian sebesar Rp4.219.138.532,00 atas persediaan 36.695 vial remikaf yang expired; beban penyisihan atas persediaan disajikan terlalu tinggi (overstated) sebesar Rp3.178.239.645,00; dan nilai persediaan disajikan terlalu tinggi (overstated) sebesar Rp18.649.427.856,00," tulis hasil pemeriksaan BPK atas pengelolaan dan pertanggungjawaban keuangan tahun 2020 sampai dengan 2022 (Semester I) pada PT Bio Farma dan anak perusahaan serta instansi terkait lainnya di DKI Jakarta dan Jawa Barat dengan nomor 56/AUDITAMA VII/PDTT/05/2023 sebagaimana diperoleh Monitorindonesia.com, Jumat (11/7/2025).
BPK juga menyatakan bahwa laporan Keuangan Kimia Farma tidak menggambarkan kondisi yang sebenarnya dan menyesatkan pengambil keputusan. Bahwa aktiva tetap disajikan terlalu tinggi minimal sebesar Rp18.649.427.856,00; ekuitas disajikan terlalu tinggi minimal sebesar Rp18.649.427.856.00; laba operasional terlalu rendah minimal sebesar Rp3.178.239.645,00; dan laba bersih terlalu tinggi Rp15.471.188.211,00.
Lebih rinci, BPK menjelaskan bahwa berdasarkan laporan keuangan Kimia Farma Induk Per 30 Juni 2022 menyayikan nilai persediaan sebesar Rp667.251.172.186,00 atau turun sebesar 18,77% dari periode 31 Desember 2021 sebesar Rp821.472.362.395,00.
Atas nilai tersebut diketahui sebesar Rp256.010.967.877,00 merupakan persediaan pada Gudang National Distribution Center (NDC) Kimia Farma.
NDC merupakan salah satu unit di bawah Divisi Supply Chain yang memiliki fungsi warehouse and distribution management, yaitu antara lain mengelola penerimaan, penyimpanan, dan pendistribusian persediaan obat Kimia Farma.
Berdasarkan hasil penghitungan, BPK menyimpulkan adanya penyimpangan-penyimpangan berindikasi tindak pidana yang dilakukan oleh pihak-pihak terkait.
1. 36.695 vial remikaf kadaluarsa
BPK menyatakan bahwa pembelian atas vial remikaf merugikan Kimia Farma minimal sebesar Rp4.219.138.532,00.
Berdasarkan Berita Acara Stock Opname NDC per 30 Juni 2022 Nomor 056/PAN/LOG/VII/2022 tanggal 8 Juli 2022 diketahui bahwa persediaan obat yang expired dan rusak adalah sebesar Rp39.213.845.513.00, atas persediaan tersebut diantaranya sebesar Rp4.219.138.532.00 merupakan obat Remukaf yang expired.
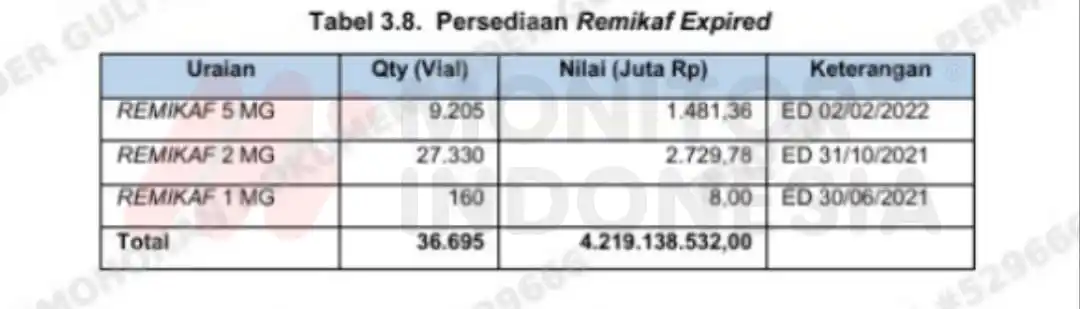
Penelusuran atas dokumen persediaan, pembelian, dan penjualan diketahui bahwa remikaf memifentanil merupakan obat analgesik anestesi produksi Laboratorio Reig Jofre, S.A., Spanyol yang mulai dipasarkan oleh Kimia Farma pada tahun 2019.
Pembelian dan penjualan Remtkaf dilakukan berdasarkan hasil analisis pasar Divisi Marketing dan Div isi New Product Development, yang menunjukkan bahwa obat-obatan analgesik anestesi memitliki value yang cukup besar di pasar Indonesia.
Adapun kelebihan dari remikaf sebagaimana dituangkan dalam analisis tersebut adalah memiliki durasi kerja yang singkat dan recovery cepat, mudah ditutrasi sesuai dengan kebutuhan operasi, tidak perlu penyesuaian dosis untuk pasien gangguan ginjal dan hati, dosis yang digunakan lebih kecil dan Fentanyl, dengan potensi analgesik dua kali lebih besar dibandingkan dengan Fentanyl, dan sebagai satu-satunya perusahaan yang memasarkan Remifentanil.
Sedangkan kelemahan dari Remikaf salah satunya adalah shelf fife yang pendek, kompetensi field force belum optimal (belum memiltki product knowledge), Dokter Anastesi yang pernah menggunakan Remifentanv! sedikit, memerlukan keterampilan dokter anastesi dalam menggunakan Remifentanyl, untuk menggunakan Remikaf harus dibantu dengan alat yaitu syringe pump atau Target Controlled Infussion (TCD, dimana alat tersebut belum tersedia di seluruh Rumah Saku, dan Remikaf belum masuk dalam standardisasi rumah sakit.
Atas hasil analisis pasar tersebut Kimia Farma melakukan perjanjian kerjasama lisensi dan pemasokan dengan Reig Jofre pada tanggal 22 Januari 2015 dan melakukan pemesanan melalui Purchase Order (PO) Remikaf sebanyak 17.000 dus atau 85.000 vial senilai Rp2.135.225.330,00.
Dalam pelaksanaan penjualan remikaf di Indonesia terdapat beberapa kendala yang dialami oleh Marketing Kimia Farma sehingga target penjualan tidak dapat dicapai.
Hal tersebut dapat dilihat dengan adanya pengembalian (retur) stok Remikaf dari Kimia Farma Trading and Distribution yang mendekati expired maupun dari Remikaf yang expired di Gudang Rusak NDC.
"Total Remikaf yang expired tersebut adalah sebanyak 7.339 dus atau 36.695 vial senilai Rp4.219.138.532,00," jelas BPK.
Manager Marketing and Sales Kimia Farma pada tanggal 27 Desember 2022 menyatakan bahwa sisa stok Remikaf yang tidak terjual dan expired disebabkan marketing Kimia Farma mengalami kesulitan dalam melakukan penetrasi pasar dimana banyak dokter anastesi yang belum terbiasa menggunakan produk Remikaf.
Selain itu berdasarkan forecasting awal kuantitas yang direncanakan akan dijual sangat besar sedangkan masa expired date Remikaf adalah singkat.
Kemudian rencana Remikaf untuk masuk dalam Formularium Nasional (Fornas), yaitu daftar obat yang disusun oleh Komite Nasional yang ditetapkan olch Kementerian Kesehatan baru dapat terlaksana pada tahun 2022. Saat ini Remikaf masih dipasarkan oleh Kimia Farma dan laku teryual namun belum menjadi produk pareto atau unggulan Kimia Farma.
2. Selisih pencatatan remikaf Rp 3,17 miliar
BPK menemukan selisih atas pencatatan persediaan remikaf dengan harga pembelian sebesar Rp3.178.239.645,00.
Surat Keputusan Direksi Nomor KEP.134 DIR XII 2016 tanggal 20 Desember 2016 tentang Metode Penilaian Persediaan mencrangkan bahwa persediaan pada NDC dinilai berdasarkan harga perolehan atau realisasi neto mana yang lebih rendah.
Namun berdasarkan penelusuran atas persediaan Remihuf yang telah expired diketahui bahwa nilai persediaan tidak dinilai berdasarkan harga perolehannya.
"Sehingya, terdapat perbedaan atau selisih — sebesar Rp3.178.239.645,00 antara persediaan dengan nilai pembelian (PO), dimana persediaan remikaf memiliki nilai yang lebih tinggi (overstated) bila dibandingkan dengan PO," beber BPK.
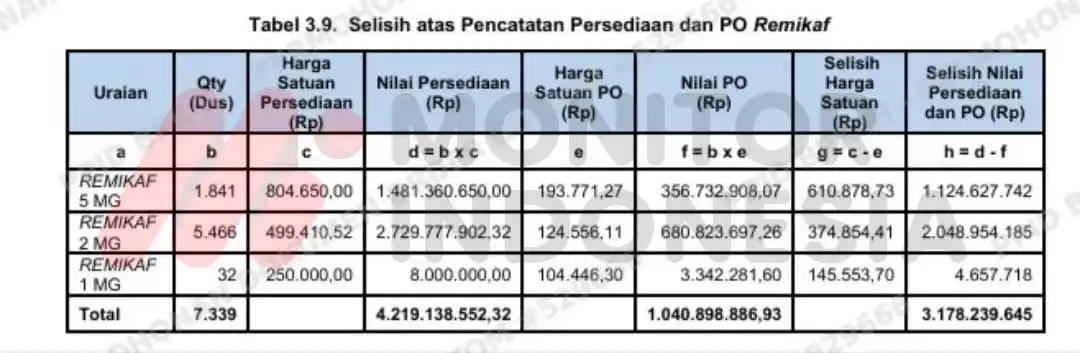
Atas persediaan remikaf yang telah expired tersebut Kimia Farma telah melakukan penyisihan atas persediaan dengan melakukan pencatatan pada beban penyisihan sebesar Rp3.178.239.645.00.
GM Akuntansi dan Keuangan Kimia Farma pada tanggal 7 Februan 2023 menjelaskan bahwa perbedaan pencatatan tersebut terjadi disebabkan oleh adanya kesalahan pencatatan harga remikaf pada master maternal pada Sistem SAP, dimana harga yang diinput adalah Harga Eceran Tertinggi (HET) yang berasal dari Divisi Marketing dan Divisi NPD bukan harga perolehan PO.
Atas hal tersebut, pencatatan Remika/ pada persediaan dan terakhir pada beban penyisihan menjadi lebih tinggi dibandingkan PO sebesar Rp3.178.239.645,00.
3. Selisih pencatatan fentanyl dan durogesic Rp 18,6 miliar
BPK menemukan selisih atas pencatatan persediaan Fentanyl dan Durogesic dengan harga pembelian senilai Rp18.649.427.856.00
Penelusuran lebih lanjut atas persediaan dilakukan secara uji petik terhadap 90 dari 367 PO obat jadi impor yang dipesan selama tahun 2020 sampai dengan Semester 2022.
"Atas hasil uji petik tersebut diketahui terdapat perbedaan atas pencatatan persediaan bila dibandingkan dengan nilai PO sebesar Rp18.649.427.856.00," jelas BPK.
Perbedaan pencatatan tersebut terjadi atas persediaan narkotika Fentanyi dan Durogesic, yaitu obat jadi impor yang masuk dalam lingkup kerja sama impor, penjualan, dan distribusi antara Kimia Farma dengan PT Johnson & Johnson Indonesia (selanjutnya disebut JJI), dan Janssen Pharmaceutica Belgia (selanjutnya disebut JP) ditandatangani pada 7 Mei 2007.
JP bermaksud untuk menjual dan mendistribusikan produknya yang bersifat narkotika di wilayah teritorial Indonesia, dengan menunjuk Kimia Farma untuk mengimpor (importir), mengemas kembali. mendistribusikan dan menyual produk (distributor), yang kegiatan pemasarannya akan dilakukan oleh JJ. Kimia Farma selama periode perjanjian akan membeli semua produk secara cksklusif dari JP atau dari pihak ketiga yang ditentukan oleh JP sesuai permintaan JJI selaku marketing produk.
Pembelian produk dan biaya impor produk JP oleh Kimia Farma dibiayai dengan sumber dana dari JJI.
Atas penunjukan Kimia Farma sebagai importir dan distributor Produk, JP akan memberikan imbalan kepada Kimia Farma seyumlah 27,5 % dari Harga Netto Apotek (HINA), yang terdiri atas imbalan pelaksanaan impor, imbalan pengepakan, imbalan penyimpanan, dan imbalan distribusi.
Penentuan HNA dilakukan secara bersama-sama oleh JP dan/atau JJI dan setiap ada perubahan harga akan dibentahukan kepada Kimia Farma.
Atas hal tersebut Kimia Farma akan melakukan update nilai persediaan berdasarkan HNA setelah dikurangi dengan imbalan sebesar 27,5%.
"Sehingga nilai persediaan atas fentanyl dan durogesic tidak menggunakan harga perolehan sebagaimana diatur dalam PSAK maupun aturan Kima Farma, namun berdasarkan harga jual HINA setelah dikurangi dengan imbalan sebesar 275%," ungkap BPK.
Adapun kondisi-kondisi tersebut disebabkan oleh kebijakan Kimia Farma dengan mclakukan penilaian persediaan berdasarkan Harga Netto Apotik dan bukan harga perolehan, namun tidak sesuai dengan dengan prinsip-prinsip yang berlaku umum.
Dan disebakan oleh Direktur Utama Kimia Farma belum melakukan evaluasi atas perjanjian kerjasama Fentanyl dan Durogesic dengan JJI, dan JP walau secara bisnis tdak menguntungkan.
Atas permasalahan tersebut, Direktur Utama Kimia Farma menyatakan menerima temuan pemeriksaan dan akan menindaklanjuti sesuai rekomendasi BPK.
Adapun BPK merekomendasikan kepada Direksi Bio Farma agar memerintahkan Direktur Utama Kimia Farma mengevaluasi fungsi dan kewajiban Direktur Keuangan dan Manajemen Risiko dan Direktur Produksi dan Supply Chain terkait kewenangan penetapan harga persediaan.
Lalu, meminta Kantor Akuntan Publik untuk mengevaluasi seluruh persediaan pada Kimia Farma dengan menelusuri nilai persediaan yang dicatat berdasarkan Harga Netto Apotik, menyesuaikannya dengan kebyakan harga perolehan, dan melakukan penyesuaian terhadap akun terdampak dalam laporan keuangan;
Kemudian melakukan evaluasi perjanjian kerjasama dengan JJI dan JP untuk memperoleh skema yang lebih menguntungkan,
BPK juga merekomendasikan kepada Direksi Bio Farma agar mengidentifikasi perjanjian kerjasama dengan pihak ketiga lainnnya yang memiliki pola kerja sama yang identik dengan JJI dan JP dan kemudian mengevaluasinya untuk memperoleh skema yang lebih menguntungkan serta memastikan seluruh kebijakan dan praktik akuntansi pada Kimia Farma sesuai dengan prinsip-prinsip yang berlaku umum.
Hingga tenggat waktu berita ini diterbitkan, Corporate Secretary (Corsec) PT Kimia Farma, Hilda, belum memberikan respons atas konfirmasi Monitorindonesia.com soal apakah semua rekomendasi BPK telah dilaksanakan.

